một muối sunfat của kim loại hóa trị (2) để lâu ngày trong không khí trở thành phân tủ muối ngậm nước.Trong phân tử muối ngậm nước kim loại chiếm 25,6 phần trăm.Tìm công thức phân tử muối ngậm nước đá
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi công thức muối ngậm nước có dạng: RSO 4 . nH 2 O
Theo đề bài ta có hệ phương trình:
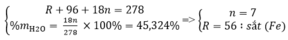
Vậy công thức của muối sắt là: FeSO 4 . 7 H 2 O

%R = R/(R+96+18n) *100% = 29.787%
<=> R = 0.29787( R + 96 +18n)
<=> R = 0.29787R + 28.595552 + 5.36166n
<=> 0.702313R - 5.36166n = 28.59552
BL :
n = 2 => R = 56
Vậy: CTHH : FeSO4 . 2H2O

Đáp án B:
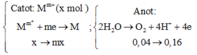
Bảo toàn electron :
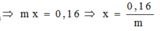
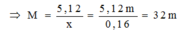
Thử lần lượt ta được M là Cu
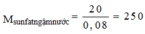
⇒ muối la CuSO4.5H2O

Hướng dẫn giải:
RO + H2SO4 → RSO4 + H2O
0,04 ←0,04
→ Oxit: FeO (72)
CTPT muối ngậm nước là: RSO4.nH2O
n = 0,04 và m = 7,52
=> M = 188
=> n = 2
=> FeSO4 . 2H2O
Vậy CTPT muối ngậm nước là: FeSO4.2H2O

Gọi công thức của muối ngậm nước có dạng RSO4.nH2O
Theo đề bài , ta có hệ phương trình :
\(\left\{{}\begin{matrix}R+96+18n=278\\\%H_2O=\dfrac{18n}{278}\cdot100\%=45,324\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n=7\\R=56\end{matrix}\right.\)
Vậy công thức của muối sunfat trên là FeSO4.7H2O

CTHH: R(NO3)2.xH2O (A)
\(\%m_{NO_3^-}=100\%-42,1875\%-9,375\%=48,4375\%\)
Xét \(\dfrac{m_R}{m_{NO_3^-}}=\dfrac{1.M_R}{2.62}=\dfrac{9,375\%}{48,4375\%}\)
=> MR = 24 (g/mol)
=> R là Mg
(A) có CTHH là Mg(NO3)2.xH2O
Có: \(\%m_{H_2O}=\dfrac{18x}{148+18x}.100\%=42,1875\%\)
=> x = 6
=> CTHH: Mg(NO3)2.6H2O

Gọi CTTQ của oxit: MO
nH2SO4 = 0,08 mol
Pt: MO + H2SO4 --> MSO4 + H2O
.....0,08<--0,08-------> 0,08................(mol)
Ta có: 0,08.(M + 16) = 4,48
=> M = 40
=> M là Canxi (Ca)
=> CTPT oxit: CaO
Gọi CTTQ muối ngậm nước: CaSO4.nH2O
ntinh thể = nCaSO4 = 0,08 mol
Ta có: 0,08.(136 + 18n) = 13,76
=> n = 2
=> CTPT muối ngậm nước: CaSO4.2H2O
Gọi công thức phân tử ngậm nước là: \(RSO_4.nH_2O\)
Đề bài quá mơ hồ . Phiền em xem lại đề bài rồi
cô em chỉ cho vậy thôi ,em bt sao bây giờ