Đốt cháy hoàn toàn một lượng hỗn hợp gồm etyl axetat và etyl propionat, thu được 15,68 lít khí CO2 (đktc). Khối lượng H2O thu được là
A. 12,6 gam
B. 50,4 gam
C. 25,2 gam
D. 100,8 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
Toàn bộ các chất ban đầu đều có CTTQ dạng C n H 2 n O 2
⇒ Khi đốt cho n C O 2 = n H 2 O = 0 , 7 m o l
⇒ m H 2 O = 12 , 6 g a m

Giải thích:
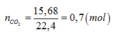
etyl axetat và etyl propionat có cùng CTPT C3H6O2 => khi đốt cháy cho số mol H2O = số mol CO2
=> nH2O = nCO2 = 0,7 (mol)
=> mH2O = 0,7.18 = 12,6 (g)
Đáp án C

Chọn đáp án D
X gồm các este no, đơn chức, mạch hở nên n C O 2 = n H 2 O = 0 , 6 m o l
⇒ V = 13,44

Chọn đáp án C
etyl axetat có công thức C H 3 C O O C 2 H 5 hay C 4 H 8 O 2
C 4 H 8 O 2 + 5 O 2 → t 0 4 C O 2 + 4 H 2 O

Chọn đáp án C
Vì X chỉ chứa các chất có dạng CnH2nO2
⇒ Khi đốt luôn cho ta n C O 2 = n H 2 O = 0 , 45 m o l
BTKL của este ta có m E s t e = m C + m H + m O
⟺ m E s t e = 0 , 45 × 12 + 0 , 45 × 2 + 0 , 16 × 2 × 16 = 11 , 42 g a m
Vì 0,16 mol X ứng với 11,42 gam
⇒ 0,2 mol X có khối lượng là: 0 , 2 × 11 , 42 0 , 16 = 14 , 27

Etyl acrylat (C5H8O2): CH2 = CH – COOC2H5
Etyl axetat (C4H8O2): CH3COOC2H5
Metyl propionat (C4H8O2): C2H5COOCH3
Quy đổi hỗn hợp thành: C5H8O2 và C4H8O2
nH2O = 1,2 mol
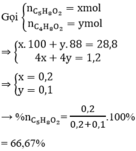
Đáp án cần chọn là: B
Chọn A