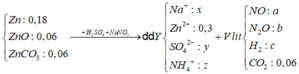
Cho 24,06 gam hỗn hợp X gồm Zn, ZnO, Z n C O 3 có tỉ lệ số mol tương ứng là 3:1:1 tan hoàn toàn trong dung dịch Y gồm H 2 S O 4 v à N a N O 3 thu được dung dịch Z chỉ chứa 3 muối trung hòa và V lít khí T (đktc) gồm N O , N 2 O , C O 2 v à H 2 . (Biết tỉ khối hơi của T so với H2 là 218/15). Cho dung dịch BaCl2 dư vào dung dịch Z, đến khi các phản ứng xảy ra hoàn toàn thu được 79,22 gam kết tủa. Còn nếu cho Z tác dụng với lượng dư dung dịch NaOH thì lượng NaOH đã phản ứng là 1,21 mol. Giá trị của V gần nhất với giá trị nào sau đây?
A. 3,5
B. 4,0
C. 4,5
D. 3,0




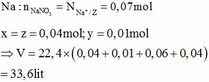

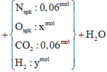




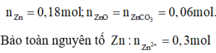

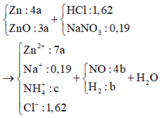
Đáp án A
Dễ tìm được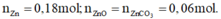
Bảo toàn nguyên tố Zn: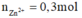
Bảo toàn nguyên tố Zn: n N a 2 Z n O 2 = 0,3 mol
Bảo toàn nguyên tố Na: n N a N O 3 = n N a + / Z = 0 , 07 m o l
Bảo toàn điện tích: n N H 4 + = 0 , 1 m o l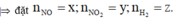
Bảo toàn nguyên tố Nitơ: 0,07 = 0,01 + x + 2y
=> m T = 30x + 44y + 0,06.44 + 2z = 218/15x2 + (x+y+0,06+z)
Lại có:
n H + =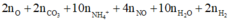
=> 0,68 = 2x0,06 + 2x0,06 + 10x0,01 + 4x + 10y + 2z
=> giải hệ ta có:
x = z = 0,04 mol; y = 0,01 mol
=> V = 22,4.(0,04 + 0,01 + 0,06 + 0,04) = 33,6 lít