Cho hỗn hợp Cu, Fe vào dung dịch HNO3 loãng. Sau phản ứng dung dịch thu được chỉ chứa một chất tan duy nhất. Chất tan đó là
A. HNO3
B. Fe(NO3)3
C. Fe(NO3)2
D. Cu(NO3)2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Coi hh X gồm Fe, Cu và O
Đặt \(n_{Fe\left(Fe_xO_y\right)}=a;n_{Cu}=b;n_{O\left(Fe_xO_y\right)}=c\) ( mol )
\(\Rightarrow m_{hh}=56a+64b+16c=14,64\left(g\right)\) (1)
\(m_{muối}=m_{Fe\left(NO_3\right)_3}+m_{Cu\left(NO_3\right)_2}=242a+188b=47,58\left(g\right)\) (2)
Bảo toàn e: \(3n_{Fe}+2n_{Cu}=2n_O+3n_{NO}=3a+2b=2c+3.0,09\) (3)
\(\left(1\right);\left(2\right);\left(3\right)\Rightarrow\left\{{}\begin{matrix}a=0,15\\b=0,06\\c=0,15\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{0,06.64}{14,64}.100=26,22\%\)
\(\dfrac{x}{y}=\dfrac{0,15}{0,15}=\dfrac{1}{1}\Rightarrow CTHH:FeO\)

Sau phản ứng thu được chất rắn Y
=> Y là Fe
Vậy X chứa Fe(NO3)2

Đáp án:C
Kim loại dư là Cu nên HNO3 hết. Vì kim loại dư nên dung dịch chỉ chứa Fe2+

Chọn đáp án D
Y có thể hoà tan được Cu và Fe sinh ra NO ⇒ Còn dư H+ và N O 3 - trong Y
⇒ Dung dịch Y gồm: Fe3+, H+, N O 3 - và S O 2 -

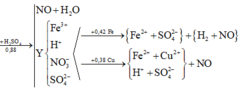
Y hoà tan tối đa 0,42 mol Fe nhưng chỉ hoà tan tối đa 0,38 mol Cu, sự chênh lệch này là do Cu không tác dụng với H+ tạo H2, đặt Z là dung dịch sau khi Y phản ứng với Cu


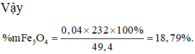

Đáp án : C
Chỉ có 1 chất tan và có kim loại dư => chứng tỏ chỉ có Fe2+

Đáp án C

→ Chất tan duy nhất trong dung dịch là Fe(NO3)2
→ Kim loại dư chắc chắn là Cu có thể có Fe.
Đáp án : C