Khi nhỏ từ từ đến dư dung dịch HCl vào dung dịch hỗn hợp gồm a mol NaOH và b mol NaAlO2, kết quả thí nghiệm được biểu diễn bằng đồ thị sau:
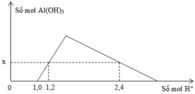
Tổng giá trị (a + b) là
A. 0,5.
B. 1,5.
C. 0,7.
D. 1,7.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Thứ tự phản ứng: H+ + OH- → H2O
H+ + AlO2- + H2O → Al(OH)3
3H+ + Al(OH)3 → Al3+ + 3H2O
- Tại: nH+ = 1,0 mol => bắt đầu có kết tủa => Phản ứng trung hòa hoàn toàn => nOH = 1 mol = a
- Tại nH+ = 1,2 mol => chưa có hiện tượng hòa tan kết tủa => nAl(OH)3 = nH+ pứ = 1,2 – 1 = 0,2 mol
- Tại nH+ = 2,4 mol => có hiện tượng hòa tan 1 phần kết tủa => nAl(OH)3 = 1/3.(4nAlO2 – nH+ pứ)
=> 0,2 = 1/3.[4b – (2,4 – 1,0)] => b = 0,5 mol
=> (a + b) = 1,5 mol

Đáp án C
Từ đồ thị dễ dàng thấy được nNaOH = x = 0,6 mol.
Tại thời điểm nHCl = 0,8 mol ta thấy nAl(OH)3 = 0,2 mol.
Ta có nAlO2– chưa tạo kết tủa = 1 , 6 - 0 , 8 4 = 0 , 2
⇒ ∑nAlO2– = 0,2 + 0,2 = y = 0,4 mol.
⇒ nNaAlO2 = 0,4 mol ⇒ x + y = 1 mol

Đáp án C
Từ đồ thị dễ dàng thấy được
nNaOH = x = 0,6 mol.
Tại thời điểm nHCl = 0,8 mol
Ta thấy nAl(OH)3 = 0,2 mol.
Ta có:
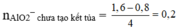
⇒ ∑nAlO2– = 0,2 + 0,2 = y = 0,4 mol.
⇒ nNaAlO2 = 0,4 mol
⇒ x + y = 1 mol

Giải thích:
Tại nNaOH = 0,8 mol thì bắt đầu có kết tủa xuất hiện
⇒ H+ trung hòa vừa hết ⇒ nHCl = a = 0,8 mol
Tại nNaOH = 2,0 và 2,8 mol thì cùng thu được lượng kết tủa như nhau
+) nNaOH = 2,0 mol thì Al3+ dư
+) nNaOH = 2,8 mol thì kết tủa tan 1 phần:
nAl(OH)3 = 4nAl3+−(nOH − nHCl) ⇒ nAlCl3 = b = 0,6 mol
Đáp án B
Đáp án B
Thứ tự phản ứng: H+ + OH- → H2O
H+ + AlO2- + H2O → Al(OH)3
3H+ + Al(OH)3 → Al3+ + 3H2O
- Tại: nH+ = 1,0 mol => bắt đầu có kết tủa => Phản ứng trung hòa hoàn toàn => nOH = 1 mol = a
- Tại nH+ = 1,2 mol => chưa có hiện tượng hòa tan kết tủa => nAl(OH)3 = nH+ pứ = 1,2 – 1 = 0,2 mol
- Tại nH+ = 2,4 mol => có hiện tượng hòa tan 1 phần kết tủa => nAl(OH)3 = 1/3.(4nAlO2 – nH+ pứ)
=> 0,2 = 1/3.[4b – (2,4 – 1,0)] => b = 0,5 mol
=> (a + b) = 1,5 mol