Cho 0,96 gam bột Mg vào 100ml dung dịch hỗn hợp gồm AgNO3 0,2M và Cu(NO3)2 1M. Khuấy đều đến phản ứng hoàn toàn thu được chất rắn A và dung dịch B. Sục khí NH3 dư vào B, lọc lấy kết tủa đem nung ở nhiệt độ cao đến khối lượng không đổi thì thu được chất rắn có khối lượng là:
A. 2,4g.
B. 1,52g.
C. 1,6g.
D. 1,2g.



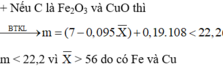
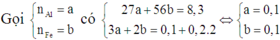
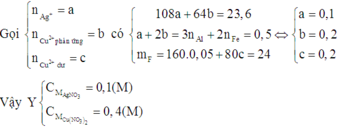
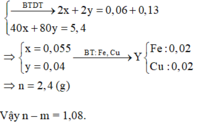


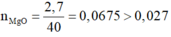
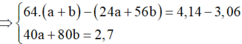
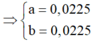
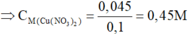
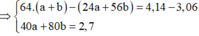
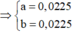
Đáp án C
nMg = 0,04. Thứ tự các phản ứng xảy ra:
Do đó dung dịch B có chứa 0,04 mol Mg(NO3)2 và Cu(NO3)2 dư.
Khi cho NH3 dư vào B thu được kết tủa duy nhất là Mg(OH)2 (Cu(OH)2 tạo phức tan được NH3)
Đem nung kết tủa thì được chất rắn là MgO. Có nMgO = n M g ( N O 3 ) 2 = 0,04
Vậy mMgO = 1,6 (gam)