Cho 9,7 gam hỗn hợp X gồm axit axetic và axit A có công thức C m H 2 m + 1 COOH tác dụng với dung dịch NaOH 1M thì vừa hết 150 ml. Xác định công thức phân tử của A. Biết tỉ lệ số mol của axit axetic và A trong hỗn hợp là 2 : 1
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khối lượng của axit axetic là 60 x 0,1 = 6 (gam).
Phần trăm khối lượng của CH 3 COOH là : 6/9,7 x 100% ≈ 61,86%
Phần trăm khối lượng của C 2 H 5 COOH là : 100% -61,86% = 38,14%

Gọi số mol của axit axetịc trong hỗn hợp là x.
Số mol của axit C n H 2 n + 1 COOH trong hỗn hợp là 2x.
Phương trình hoá học của phản ứng giữa X với NaOH
CH 3 COOH + NaOH → CH 3 COONa + H 2 O
x mol x mol
C n H 2 n + 1 COOH + NaOH → C n H 2 n + 1 COONa + H 2 O
2x mol 2x mol
Theo đầu bài ta có :
n NaOH = 300/1000 x 1 = 0,3 mol
Theo phương trình : x + 2x = 0,3 → x = 0,1 (mol)
Khối lượng của CH 3 COONa là : 0,1(15 + 44+ 23) = 8,2 (gam).
Khối lượng của C n H 2 n + 1 COONa là: 0,2(14n + 68) = (2,8n + 13,6).
Theo đề bài : 8,2 + 2,8n + 13,6 = 27,4
Vậy : 2,8n = 27,4 - 21,8 = 5,6.
→ n = 2. Công thức của axit là C 2 H 5 COOH.

Phương trình hoá học :
C n H 2 n + 1 COOH + NaOH → C n H 2 n + 1 COONa + H 2 O
Gọi số mol của hai axit trong hỗn hợp là x.
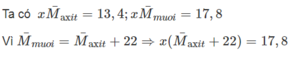
13,4 + 22x = 17,8 => x = 0,2 => số mol của mỗi axit trong hỗn hợp là 0,1
Ta có công thức của 2 axit là C a H 2 a + 1 COOH (0,1 mol)
C b H 2 b + 1 COOH (0,1 mol)
Vậy : (14a + 46)0,1 + (14b + 46)0,1 = 13,4
=> 14a + 14b = 42 => a + b = 3
a = 1; b = 2 → CH 3 COOH và C 2 H 5 COOH
m CH 3 COOH = 0,1 x 60 = 6g
m C 2 H 5 COOH = 0,1 x 74 = 7,4g
% m CH 3 COOH = 6/13,4 x 100% ≈ 44,8%
% m C 2 H 5 COOH = 100% - 44,8% = 55,2%
n NaOH = n CH 3 COOH + n C 2 H 5 COOH = 0,2 mol
V = n : C M = 0,2 : 1 = 200ml

Ta có khối lượng axit axetic là : 60 x 0,1 = 6 (gam).
Khối lượng C 2 H 5 COOH là : 74 x 0,2 = 14,8 (gam).
Vậy m hh : (6 + 14,8) = 20,8 (gam).
→ % khối lượng axit axetic : 6/20,8 x 100% = 28,85%
% khối lượng C 2 H 5 COOH : 100 - 28,85 = 71,15 (%).

Gọi số mol axit axetic trong hỗn hợp là x.
Số mol rượu etylic trong hỗn hợp là y.
Phương trình hoá học của phản ứng khi X tác dụng với Na :
2 CH 3 COOH + 2Na → 2 CH 3 COONa + H 2 ↑
x mol x/2 mol
2 C 2 H 5 OH + 2Na → 2 C 2 H 5 ONa + H 2
y mol y/2 mol
Ta có: n H 2 = x/2 + y/2
Theo đề bài : n H 2 = 0,336/22,4 = 0,015 mol
Vậy x/2 + y/2 = 0,015 → x + y = 0,03 mol
Phương trình hoá học của phản ứng khi X tác dụng với NaOH :
CH 3 COOH + NaOH → CH 3 COONa + H 2 O
x x
Theo đề bài số mol NaOH phản ứng là 0,1 x 0,2 = 0,02 (mol).
Vậy x = 0,02 (mol) và y = 0,03 - x = 0,03 - 0,02 = 0,01 (mol).
→ Khối lượng hỗn hợp là m = 0,02 x 60 + 0,01 x 46 = 1,2 + 0,46 = 1,66 (gam)

CH 3 COOH + NaOH → CH 3 COONa + H 2 O
C n H 2 n + 1 COOH + NaOH → C n H 2 n + 1 COONa + H 2 O

Đáp án A
10,36 gX + 0,12 mol HCl → X có 0,12 mol NH2→ mN(X) = 1,68 g → mO(X) =1,68:7.16 = 3,84 g
nO =0,24 mol → nCOOH = 0,24 :2 =0,12 mol
X chứa 0,12 mol COOH + 0,15 mol NaOH → 0,12 mol H2O
Áp dụng định luật bảo toàn khối lượng
mX +mNaOH = mrắn + mH2O → mrắn = 10,36 + 0,15.40-0,12.18=14,2
Đáp án A
Chú ý:
Sai lầm và chú ý:
Trong rắn thu được có cả muối và NaOH

10 , 36 g X + 0 , 12 m o l H C l → X c ó 0 , 12 m o l N H 2
→ m N ( X ) = 1 , 68 g a m → m O ( X ) = 1 , 68 7 .16 = 3 , 84 g a m
n O = 0 , 24 m o l → n C O O H = 0 , 24 : 2 = 0 , 12 m o l
X chứa 0,12 mol COOH + 0,15 mol NaOH → 0 , 12 m o l H 2 O
Áp dụng định luật bảo toàn khối lượng
m X + m N a O H = m r a n + m H 2 O → m r a n = 10 , 36 + 0 , 15.40 − 0 , 12.18 = 14 , 2 g a m
Đáp án cần chọn là: A
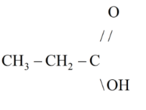
Gọi số mol của CH 3 COOH trong hỗn hợp là 2x.
Vậy số mol của C m H 2 m + 1 COOH trong hỗn hợp là x.
Ta có : 2x x 60 + x(14m + 46) = 9,7 (1)
Phương trình hoá học của phản ứng giữa X với NaOH :
CH 3 COOH + NaOH → CH 3 COONa + H 2 O
C m H 2 m + 1 COOH + NaOH → C m H 2 m + 1 COONa + H 2 O
Theo phương trình: n NaOH = n axit = 2x + x = 3x = 0,15 mol
⇒ x = 0,05
Thay x = 0,05 vào phương trình (1), ta có :
2 x 0,05 x 60 + 0,05(14m + 46) = 9,7.
→ 0,7m + 6 + 2,3 = 9,7.
→ m = 2.
Công thức của axit phải tìm là C 2 H 5 COOH.