Cho 69,6 gam MnO2 tác dụng với HCl đặc, dư.(H%=90%). Dẫn toàn bộ lượng khí sinh ra vào 500 ml dung dịch NaOH 4M thu được dung dịch A. Coi thể tích dung dịch thay đổi không đáng kể, nồng độ mol các chất trong dung dịch A sau phản ứng là bao nhiêu?
A. 1,6M; 1,6M và 0,8M
B. 1,7M; 1,7M và 0,8 M
C. 1,44M; 1,44M và 1,12 M
D. 1,44M ; 1,44M và 0,56M


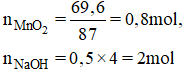
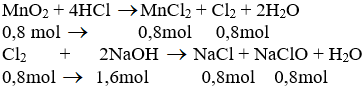
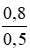 = 1,6 mol/ lit
= 1,6 mol/ lit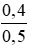 = 0,8 mol/ lit
= 0,8 mol/ lit
Đáp án C
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,8 →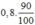 = 0,72 (mol)
= 0,72 (mol)
Vkhí = 0,72.22,4 = 16,128 (lit)
nNaOH = 2 (mol)
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,72 2 → 0,72 0,72 (mol)
do NaOH dư, tính theo Cl2
Dung dịch sau phản ứng: nNaCl = nNaClO = 0,72 (mol)
nNaOH dư = 0,56 (mol)
CNaCl = CNaClO = 1,44M, CNaOH = 1,12M