Nhiệt phân hoàn toàn 25,9 gam muối hiđrocacbonat của một kim loại R có hóa trị II không đổi. Khí thoát ra được hấp thụ hết vào bình đựng dung dịch nước vôi trong dư thu được 20 gam kết tủa. Kim loại R là
A. Cu
B. Mg
C. Ba
D. Ca.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giả sử kim loại hóa trị II là A.
Ta có: nBa(OH)2 = 0,1 (mol)
nBaCO3 = 0,05 (mol)
\(ACO_3\underrightarrow{t^o}AO+CO_2\)
- TH1: Ba(OH)2 dư.
PT: \(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
Theo PT: \(n_{ACO_3}=n_{CO_2}=n_{BaCO_3}=0,05\left(mol\right)\)
\(\Rightarrow M_{ACO_3}=\dfrac{15}{0,05}=300\left(g/mol\right)\Rightarrow M_A=240\left(g/mol\right)\)
→ Không có chất nào thỏa mãn.
- TH2: Ba(OH)2 hết.
PT: \(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
______0,05_____0,05_____0,05 (mol)
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\)
___0,05_____0,1 (mol)
⇒ nCO2 = 0,05 + 0,1 = 0,15 (mol)
Theo PT: \(n_{ACO_3}=n_{CO_2}=0,15\left(mol\right)\Rightarrow M_A=\dfrac{15}{0,15}=100\left(g/mol\right)\)
\(\Rightarrow M_A=40\left(g/mol\right)\)
→ A là Ca.
Vậy: CTHH cần tìm là CaCO3

Đáp án D
Gọi công thức của muối cacbonat đem nhiệt phân là MCO3
Có phản ứng: M C O 3 → t 0 M O + C O 2
Có n N a O H = 350 . 4 % 40 = 0,35; gọi n C O 2 = x
Vì CO2 được hấp thụ hoàn toàn vào dung dịch NaOH nên có 2 trường hợp xảy ra:
+) Trường hợp 1: Sau phản ứng NaOH còn dư, sản phẩm thu được là Na2CO3.
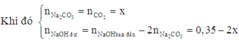
Mà dung dịch thu được có khối lượng chất tan là 20,1 gam
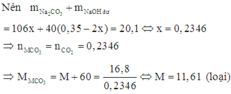
+) Trường hợp 2: Sản phẩm thu được trong dung dịch là Na2CO3 và NaHCO3
Khi đó

Mà dung dịch thu được có khối lượng chất tan là 20,1 gam nên
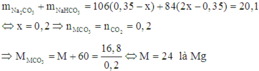
Vậy kim loại cần tìm là Mg.

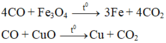
![]()
Khí thoát ra khỏi bình dẫn qua dung dịch Ca OH 2 thu được 5 gam kết tủa CaCO 3
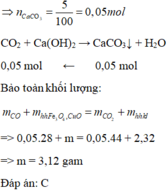

Đáp án D
Vì CO dư nên hỗn hợp sau phản ứng chỉ gồm kim loại:
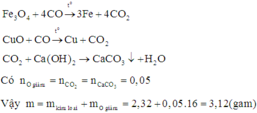

Đáp án C
Kết tủa là CaCO3 0,05 mol do đó CO2 là 0,05 mol hay O bị khử 0,05 mol
![]()
Chọn đáp án C
Bảo toàn C:
R H C O 3 2 → C O 2 → 2 C a C O 3
0,1 ← 0,2 (mol)
R H C O 3 2 = 25,9 : 0,1 = 259 => R = 137 (Ba)