Theo hướng dẫn của giáo viên, bạn Hùng đã tiến hành làm thí nghiệm: Lấymột mẫu nhỏ vôi tôi (calcium hydroxide) cỡ bằng hạt ngô cho vào cốc thuỷ tinh, cho tiếp vào cốc khoảng 50 ml nước cất và khuấy đều. Sau đó rót toàn bộ dungdịch trong cốc vào phễu lọc đã đặt trên bình tam giác. Khoảng 15 phút sau, bạnHùng thu được dung dịch trong suốt trong bình tam giác và còn một lượng vôi tôi trên phễu lọc. Bạn Hùng...
Đọc tiếp
Theo hướng dẫn của giáo viên, bạn Hùng đã tiến hành làm thí nghiệm: Lấy
một mẫu nhỏ vôi tôi (calcium hydroxide) cỡ bằng hạt ngô cho vào cốc thuỷ tinh, cho tiếp vào cốc khoảng 50 ml nước cất và khuấy đều. Sau đó rót toàn bộ dung
dịch trong cốc vào phễu lọc đã đặt trên bình tam giác. Khoảng 15 phút sau, bạn
Hùng thu được dung dịch trong suốt trong bình tam giác và còn một lượng vôi tôi trên phễu lọc.
Bạn Hùng lấy dung dịch trong bình tam giác cho vào 3 ống nghiệm, mỗi ống khoảng 1ml rồi tiếp tục thí nghiệm.
Ống nghiệm 1, bạn Hùng đun lên ngọn lửa đèn cồn đến vừa cạn. Kết quả là thu được chất rắn màu trắng chính là vôi tôi.
Ống nghiệm 2, bạn Hùng dùng ống hút và thổi nhẹ vào. Kết quả là dung dịch trong suốt bị vẫn đực do calcium hydroxide tác dụng với khí carbon dioxide sinh ra calcium carbonate (chất rắn màu trắng).
Ống nghiệm 3, bạn Hùng để trong môi trường không khí. Kết quả là sau một thời gian ống nghiệm cũng bị đục dần, có lớp váng mỏng màu trắng chính là calcium carbonate nổi trên bề mặt dung dịch.
a) Nêu một số tính chất vật lý của vôi tôi (calcium hydroxide) mà em quan sát được trong thí nghiệm.
b) Calcium hydroxide là chất tan nhiều hay tan ít trong nước?
c) Ống nghiệm nào đã thể hiện tính chất hóa học của calcium hydroxide?
d) Từ kết quả ở ống nghiệm 2 và ống nghiệm 3, em có kết luận trong không khí có chứa chất gì?



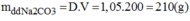
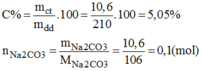
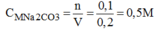
Cốc hoà tan đường saccarozơ ngọt hơn.