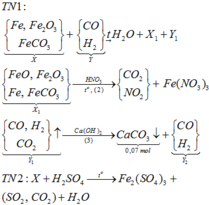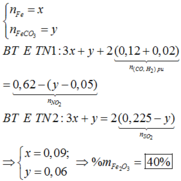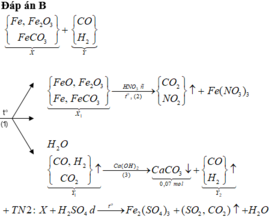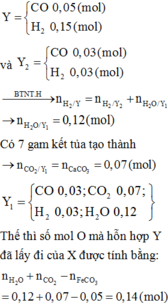Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
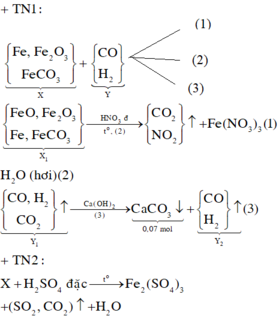
Sơ đồ quá trình phản ứng
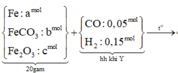
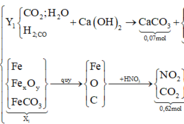

Hướng tư duy 1:
+ Xét khí Y1 có ![]()
![]()
+Xét hỗn hợp X1(sau khi quy đổi) có:
![]()
![]()
Do đó, trong 0,62 mol hỗn hợp khí có (0,67-b) mol NO (khí hóa nâu)
Bảo toàn nguyên tố Fe có:
![]()
= a + b = 2c mol
Bảo toàn O: ![]()
![]()
![]()
Bảo toàn e:
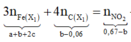
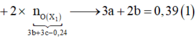
+ Xét hỗn hợp khí sau khi tác dụng H 2 S O 4 ta có:
![]()
![]()
Mà ![]()
=> giải hệ (1), (2), (3) ta được
![]()
Hướng tư duy 2:
Gọi x là số mol F e C O 3 bị nhiệt phân
Bảo toàn C ta có: ![]() = 0,05 mol
= 0,05 mol
=>
n
C
O
(
p
h
ả
n
ứ
n
g
)
= ![]()
![]()
+ Gọi a là số mol
F
e
C
O
3
phản ứng với
H
N
O
3
có ngay ![]()
+ Cho X phản ứng với H 2 S O 4 (đặc, nóng): (X chứa a+0,05 mol F e C O 3 )
Bảo toàn nguyên tố C có: ![]()
![]()
Bảo toàn e trong phản ứng với H N O 3 và H 2 S O 4 đặc nóng, có hệ:
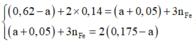
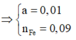
![]()
![]()

n HCl = 360 x 18,25/(100x36,5) = 1,8 mol
H 2 + CuO → t ° Cu + H 2 O
n CuO = x
Theo đề bài
m CuO (dư) + m Cu = m CuO (dư) + m Cu p / u - 3,2
m Cu = m Cu p / u - 3,2 => 64x = 80x - 3,2
=> x= 0,2 mol → m H 2 = 0,4g
Fe + 2HCl → FeCl 2 + H 2
Số mol HCl tác dụng với Fe 3 O 4 , Fe 2 O 3 , FeO là 1,8 - 0,4 = 1,4 mol
Phương trình hóa học của phản ứng:
Fe 3 O 4 + 8HCl → 2 FeCl 3 + FeCl 2 + 4 H 2 O (1)
Fe 2 O 3 + 6HCl → 2 FeCl 3 + 3 H 2 O (2)
FeO + 2HCl → FeCl 2 + H 2 O (3)
Qua các phản ứng (1), (2), (3) ta nhận thấy n H 2 O = 1/2 n HCl = 1,4:2 = 0,7 mol
Áp dụng định luật bảo toàn khối lượng, ta có:
m hỗn hợp + m HCl = m muối + m H 2 O + m H 2
57,6 + 1,8 x 36,5 = m muối + 0,7 x 18 +0,4
m muối = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)

a) Gọi \(\left\{{}\begin{matrix}n_{NO_2}=a\left(mol\right)\\n_{NO}=b\left(mol\right)\end{matrix}\right.\)
Ta lập HPT: \(\left\{{}\begin{matrix}a+b=\dfrac{3,136}{22,4}=0,14\\46a+30b=0,14\cdot19\cdot2\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,07\\b=0,07\end{matrix}\right.\)
Gọi \(n_{FeO}=n_{CuO}=n_{Fe_3O_4}=x\left(mol\right)\)
Coi hỗn hợp ban đầu gồm Fe (4x mol), Cu (x mol) và O (6x mol)
Bảo toàn electron: \(3n_{Fe}+2n_{Cu}=2n_O+n_{NO_2}+3n_{NO}\)
\(\Rightarrow12x+2x=12x+0,07+3\cdot0,07\) \(\Leftrightarrow x=0,14\)
\(\Rightarrow a=m_{hh}=72\cdot0,14+80\cdot0,14+232\cdot0,14=53,76\left(g\right)\)
b) Ta có: \(n_{HNO_3\left(p.ứ\right)}=n_{e\left(trao.đổi\right)}+n_{NO_2}+n_{NO}=0,07+0,07\cdot3+0,07+0,07=0,42\left(mol\right)\)