Một oxit của photpho có thành phần phần trăm của P bằng 43,66%. Biết phân tử khối của oxit bằng 142 đvC . Công thức hóa học của oxit là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Đặt công thức hóa học của oxit là PxOy.
Theo bài ra: 31x + 16y = 142 (1)
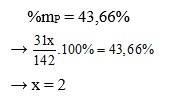
Thay x = 2 vào (1) được y = 5.
Vậy công thức hóa học của oxit là P2O5.

Gọi công thức hóa học của photpho: P x O y
%O = 100 – 43,66 = 5,34%
M P x O y = 31x + 16y = 142
Tỉ lệ khối lượng:
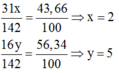
Vậy công thức hóa học của oxit photpho là P 2 O 5 .
Chọn A.

một oxit cua photpho có thành phần phần trăm của p bằng 43,66% .biết phân tử khối của oxit là 142 DVC .công thức hóa học của oxit là
A p2o5
B p2o3
C po2
D p2o4

1
Đặt CT: FexOy
Ta có:
MFe:MO=56x\16y= 21\8= 448x\336y
⇒ x\y= 3\4
⇒ x = 3 ; y = 4
⇒ CT của oxit sắt: Fe3O4
⇒ Fe3O4 có PTK: 3.56+4.16 = 232 đvC
2.
Gọi công thức hóa học của oxit photpho là PxOy
Lập các tỷ số khối lượng:
x×31\142=43,66\100→x≈2
y×16\142=56,34\100→y=5
Công thức hóa học của oxit photpho là P2O5

Câu 1 : Lưu huỳnh trioxit (SO3) tác dụng được với:
A. Nước, sản phẩm là bazơ.
B. Axit, sản phẩm là bazơ.
C. Nước, sản phẩm là axit
D. Bazơ, sản phẩm là axit.
Câu 2 : Một oxit của photpho có thành phần phần trăm của P bằng 43,66%. Biết phân tử khối của oxit bằng 142đvC. Công thức hoá học của oxit là:
A. P2O3.
B. P2O5.
C. PO2.
D. P2O4.
Câu 3 : Khử hoàn toàn 0,58 tấn quặng sắt chứa 90 % là Fe3O4 bằng khí hiđro. Khối lượng sắt thu được là:
A. 0,378 tấn.
B. 0,156 tấn.
C. 0,126 tấn.
D. 0,467 tấn.

Ta có: \(\left\{{}\begin{matrix}m_S=64\cdot50\%=32\left(g\right)\\m_O=64\cdot50\%=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_S=\dfrac{32}{32}=1\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH là \(SO_2\)

Khối lượng của các nguyên tố trong hợp chất là:
\(m_{FE}=\dfrac{70.160}{100}=112\left(g\right)\)
\(m_O=\dfrac{30.160}{100}=48\left(g\right)\)
Số mol có trong mỗi nguyên tố là:
\(n_{FE}=\dfrac{m_{FE}}{M_{FE}}=\dfrac{112}{56}=2\left(mol\right)\)
\(n_O=\dfrac{m_O}{M_O}=\dfrac{48}{16}=3\left(mol\right)\)
Vậy hợp chất có 2 nguyên tử Fe, 3 nguyên tử O
Công thức hóa học của hợp chất là: \(FE_2O_3\)

C1: Gọi CTTQ: PxOy
x = \(\frac{43,66\times 142}{31\times 100}\approx 2\)
%O = 100% - 43,66% = 56,34%
y = \(\frac{56,34\times 142}{16\times 100}= 5\)
Vậy CTHH: P2O5
C2: Gọi CTTQ: PxOy
%O = 100% - 43,66% = 56,34%
x : y = \(\frac{43,66}{31} : \frac{56,34}{16}= 1,4 : 3,5 = 2 : 5\)
Vậy CTHH: P2O5