Hòa tan 50g CuSO4 .5H2O vào 450g nước. Tính C% của dung dịch thu được. Biết độ tan của K2SO4 ở 60oC là 18,2g. Tính C% của dung dịch bão hòa ở nhiệt đọ này
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(C\%=\dfrac{11,1}{11,1+100}.100\%=9,99\%\\ m_{K_2SO_4}=200.9,99\%=20\left(g\right)\)

\(S_{CuSO_4\left(30^oC\right)}=\dfrac{75}{300}.100=25\left(g\right)\)

1,2 kg = 1200 gam
ở 80 độ C, S = 50 gam tức là :
50 gam CuSO4 tan tối đa trong 100 gam nước tạo 150 gam dd bão hòa.
Suy ra :
m CuSO4 = 1200.50/150 = 400(gam)
m H2O = 1200 - 400 = 800(gam)
Gọi n CuSO4.5H2O = a(mol)
Sau khi tách tinh thể :
m CuSO4 = 400 - 160a(gam)
m H2O = 800 - 18.5a(gam)
Ta có :
S = m CuSO4 / m H2O .100 = 15
<=> (400 - 160a) / (800 -18.5a) = 15/100
<=> a = 1,911
=> m CuSO4.5H2O = 477,75 gam

Giả sử có 100 nước
\(\rightarrow m_{K_2SO_4}=15\left(g\right)\\ \rightarrow C\%_{K_2SO_4}=\dfrac{15}{15+100}=13,06\%\)

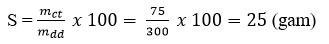
- Quy đổi:
250g CuSO4 .5H2O thì có 160g CuSO4
Vậy 50g CuSO4 .5H2O thì có 32g CuSO4
\(C\%_{CuSO_4}=\dfrac{32.100}{50+450}=6,4\%\)
- Độ tan =18,2g tức là có 18,2 g K2SO4 trong 100g nước
\(C\%_{K_2SO_4}=\dfrac{18,2.100}{18,2+100}\approx15,4\%\)