Đốt nóng hỗn hợp gồm Al và 3,48 gam Fe3O4 trong điều kiện không có oxi đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp chất rắn F có khối lượng 4,83 gam. Cho toàn bộ hỗn hợp F vào 50ml dung dịch CuSO4 1M. Sau khi phản ứng xảy ra hoàn toàn, lọc được m gam hỗn hợp chất rắn Z. Tính m.

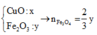
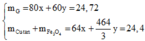

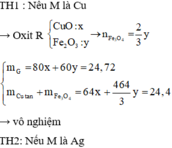
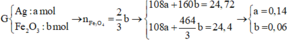


*TH1: Gỉa sử lượng Al đưa vào phản ứng lấy vừa đủ
nFe3O4 = 0,015 (mol)
8Al + 3Fe3O4 ---> 4Al2O3 + 9Fe (1)
0,04.....0,015...........0,02..........0,045 (mol)
Lượng chất rắn F thu được gồm Al2O3 (0,02 mol), Fe (0,045mol)
=> m chất rắn = 4,56 (g) < 4,83 (g)
=> Loại
*TH2: Lượng Al đưa vào phản ứng lấy dư:
nAl (bđ) = 4,83-3,48 = 1,35 (g)
=> nAl (bđ) = 0,05 (mol)
8Al + 3Fe3O4 ---> 4Al2O3 + 9Fe (2)
0,04.....0,015...........0,02..........0,045 (mol)
=> Chất rắn F gồm: Al2O3 (0,02 mol), Fe (0,045 mol), Al dư (0,01 mol)
nCuSO4 = 0,05 (mol)
2Al + 3CuSO4 ---> Al2(SO4)3 + 3Cu (3)
0,01...0,015......................................0,015
Fe + CuSO4 ---> FeSO4 + Cu (3)
0,035..0,035..........................0,035
=> m = (0,015 + 0,035 ) .64 = 3,2 (g)