Hìa tan hoàn toàn 6,66g tinh thể Al2(SO4)3.xH2O vào nước thành dung dịch A . Lấy 1/10 dung dịch A cho tác dụng với dung dịch BaCl2 dư thì thu được 0,699g kết tủa. Hãy xác định công thức của tinh thể muối sunfat nhôm ngậm nước ở trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


3BaCl2 + Al2(SO4)3→ 3BaSO4 + 2AlCl3
nBaSO4=\(\frac{0,699}{137+32+16.4}=0,003\) mol
theo PT => nAl2(SO4)3=0,001mol
vì lấy 1/10=> nAl2(SO4)3 ban đầu=0,01 mol
=>MAl2(SO4)3.nH2O=\(\frac{6,66}{0,01}=666\)
=> 27.2+3(32+16.4)+18n=666
<=>n=18
vậy công thức hidrat trên là Al2(SO4)3.18H2O

MSO4 + Ba(NO3)2 => BaSO4 + M(NO3)2
0,1 <--------------------- 0,1
nBaSO4 = 0,1mol
MSO4 + 2NaOH => Na2SO4 + M(OH)2
0,1-------------------------------------> 0,1
MM(OH)2= \(\frac{9}{0,1}\) = 90 => M=56 => Fe
=> công thức FeSO4.nH2O
n tinh thể = nFeSO4 = 0,1
=> M tinh thể = 27,8/0,1= 278
<=> 152 + 18n = 278 => n= 7
=> FeSO4.7H2O

Đáp án A
Gọi số mol Al3+, NH4+, SO42- trong 100 ml dung dịch Y lần lượt là x, y, z mol
-Phần 1:
Al3++ 3NH3+ 3H2O→ Al(OH)3+ 3NH4+
x/5 x/5 = 2.10-3 suy ra x = 0,01 mol
-Phần 2:
Ba2++ SO42-→ BaSO4
z/5 mol z/5 mol = 0,932/233 = 4.10-3 mol nên z = 0,02 mol
ĐLBT ĐT suy ra y = 0,01 mol suy ra nH2O = 0,12 mol
Suy ra CT là Al.NH4.(SO4)2.12H2O

Bài 3:
\(n_{CuSO_4}=0,2\times0,2=0,04\left(mol\right)\)
Ta có: \(n_{CuSO_4.pH_2O}=0,04\left(mol\right)\)
\(\Rightarrow M_{CuSO_4.pH_2O}=\frac{10}{0,04}=250\left(g\right)\)
\(\Leftrightarrow160+18p=250\)
\(\Leftrightarrow18p=90\)
\(\Leftrightarrow p=5\)
Bài 2:
\(n_{BaCl_2.xH_2O}=\frac{24,4}{208+18x}\left(mol\right)\)
Ta có: \(n_{BaCl_2}=n_{BaCl_2.xH_2O}=\frac{24,4}{208+18x}\left(mol\right)\)
\(\Rightarrow m_{BaCl_2}=\frac{24,4}{208+18x}\times208=\frac{5075,2}{208+18x}\left(g\right)\)
ta có: \(m_{ddBaCl_2}mới=24,4+175,6=200\left(g\right)\)
\(C\%_{BaCl_2}mới=\frac{5075,2}{208+18x}\div200\times100\%=10,4\%\)
\(\Leftrightarrow\frac{5075,2}{41600+3600x}=0,104\)
\(\Leftrightarrow5075,2=4326,4+374,4x\)
\(\Leftrightarrow748,8=374,4x\)
\(\Leftrightarrow x=2\)

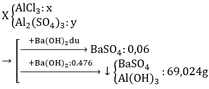
Cho Ba(OH)2 vào muối Al sẽ có 2TH sau:
TH1: kết tủa Al(OH)3 chưa bị hòa tan
Al3+ + 3OH– → Al(OH)3↓
→ nAl(OH)3 = nAl3+ → nAl(OH)3 = xn + 0,04n
TH2: kết tủa Al(OH)3 bị hòa tan một phần
Al3+ + 3OH– → Al(OH)3↓
(xn + 0,04n)→ 3(xn + 0,04n) (xn + 0,04n)
Al(OH)3 + OH– → AlO2– + 2H2O
0,952 – 3(xn + 0,04n) ←0,952
→ nAl(OH)3 = 4xn + 0,16n – 0,952


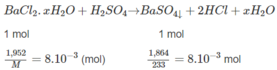
⇒ M = 244g/mol = M B a C l 2 . x H 2 O . Từ đó :
⇒ x = 2.
Đáp số : B a C l 2 . x H 2 O


Số mol kết tủa tạo thành:
n(BaSO4) = 0,699/233 = 0,003mol
Al2(SO4)3 + 3BaCl2 → 3BaSO4 + 2AlCl3
0,001 0,003
Số mol Al2(SO4)3 có trong dung dịch A:
n[Al2(SO4)3] = 0,001.10 = 0,01mol
Khối lượng mol phân tử của muối hidrat:
M[Al2(SO4)3.nH2O] = 342 + 18n = 6,66/0,01 = 666
→ n = (666-342)/18 = 18
Vậy công thức tinh thể muối nhôm sunfat là Al2(SO4)3.18H2O
Cảm ơn nhiều nha