Trong 800 ml của một dung dịch có chứa 8 g NaOH.
a) Hãy tính nồng độ mol của dung dịch này.
b) Phải thêm bao nhiêu ml nước vào 200 ml dung dịch này để được dung dịch NaOH 0,1 M ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài giải:
a) Số mol của NaOH là:
n = 0,2 mol
Nồng độ mol của dung dịch là:
CM = = 0,25 M
b. Thể tích nước cần dùng:
- Số mol NaOH có trong 200 ml dung dịch NaOH 0,25 M:
nNaOH = = 0,05 mol
Thể tích dung dịch NaOH 0,1 M có chứa 0,05 NaOH
Vdd = = 500 ml
Vậy thể tích nước phải thêm là:
= 500 – 200 = 300 ml

a)
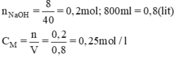
b) nNaOH có trong 200ml dung dịch NaOH 0,25M là

VH2O cần dùng để pha loãng 200ml dung dịch NaOH 0,25M để dung dịch NaOH 0,1M.
VH2O = 500 - 200 = 300ml H2O.

a) Số mol của NaOH là : n = 0,2 mol
Nồng độ mol của dung dịch A là: \(C_M=\dfrac{0,2.1000}{800}=0,25M\)
b) Thể tích nước cần dùng :
Số mol NaOH có trong 200 ml dung dịch NaOH 0,25 M:
\(n_{NaOH}=\dfrac{0,25.200}{1000}=0,05mol\)
Thể tích dung dịch NaOH 0,1 M có chứa 0,05 NaOH
\(V_{dd}=\dfrac{0,05.1000}{0,1}=500ml\)
Vậy thể tích nước phải thêm là:
\(V_{H_2O}=500-200=300ml\)

a) Ta có: 800ml=0,8 lít
nNaOH=m/M=8/40=0,2 (mol)
=> CM=\(\dfrac{n}{V}=\dfrac{0,2}{0,8}=0,25\left(M\right)\)
b) Ta có: 200ml=0,2 lít
=> nNaOH=CM.V=0,1.0,5=0,05 (mol)
Gọi x là sô gam nước cần thêm vào:
=> \(0,1=\dfrac{0,05}{x}\)
=> x=0,5 lít =500ml
Vậy cần phải thêm vào 500 - 200 =300 ml nước
a)đổi 700ml=0,8 lít
nNaOH=8/40=0,2mol
CM=n/V=0,2/0,8=0,25M
b) đổi 200ml=0,2 lít
nNaOH=0,25.0,2=0,05mol
gọi x là số gam nước cần thêm vào
=> \(0,1=\dfrac{0,05}{x}=>x=0,5\) ( lít )=500ml
Vậy cần thêm vào 500-200=300ml nước

Câu 2 :
$n_{HCl} = 0,2.1 + 0,3.1,5 = 0,65(mol)$
$V_{dd} = 0,2 + 0,3 = 0,5(mol)$
$C_{M_{HCl}} = \dfrac{0,65}{0,5} =1,3M$
Câu 3 :
Gọi $m_{H_2O\ cần\ thêm} =a (gam)$
Sau khi thêm :
$m_{NaOH} = 100.35\% = 35(gam)$
$m_{dd} = 100 + a(gam)$
Suy ra: $\dfrac{35}{100 + a}.100\% = 20\%$
Suy ra: a = 75(gam)
Câu 4 :
Gọi $V_{dd\ HCl\ 2M} =a (lít) ; V_{dd\ HCl\ 3M} = b(lít)$
Ta có :
$a + b = 4$
$2a + 3b = 4.2,75$
Suy ra a = 1(lít) ; b = 3(lít)

a)
$n_{NaCl} = 0,8.1 = 0,8(mol)$
$m_{NaCl} = 0,8.58,5 = 46,8(gam)$
Pha chế :
- Cân lấy 46,8 gam NaCl cho vào trong cốc 1 lít có chia vạch
- Đong từ từ nước vào cốc cho đến khi chạm vạch 800ml thì dừng lại, khuấy đều.
b)
$V_{dd\ sau\ khi\ thêm} = 800 + 200 = 1000(ml) = 1(lít)$
$C_{M_{NaCl}} = \dfrac{0,8}{1} = 0,8M$
c)
$n_{NaCl} = \dfrac{11,7}{58,5} = 0,2(mol)$
$n_{NaCl\ sau\ khi\ thêm} = 0,8 + 0,2 = 1(mol)$
$C_{M_{NaCl}} = \dfrac{1}{0,8} = 1,25M$
a) Số mol của NaOH là:
n = 0,2 mol
Nồng độ mol của dung dịch là:
CM =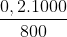 = 0,25 M
= 0,25 M
b. Thể tích nước cần dùng:
- Số mol NaOH có trong 200 ml dung dịch NaOH 0,25 M:
nNaOH =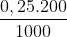 = 0,05 mol
= 0,05 mol
Thể tích dung dịch NaOH 0,1 M có chứa 0,05 NaOH
Vdd =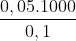 = 500 ml
= 500 ml
Vậy thể tích nước phải thêm là:
a) Số mol của NaOH là:
n = 0,2 mol
Nồng độ mol của dung dịch là:
CM =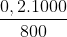 = 0,25 M
= 0,25 M
b. Thể tích nước cần dùng:
- Số mol NaOH có trong 200 ml dung dịch NaOH 0,25 M:
nNaOH =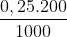 = 0,05 mol
= 0,05 mol
Thể tích dung dịch NaOH 0,1 M có chứa 0,05 NaOH
Vdd =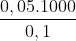 = 500 ml
= 500 ml
Vậy thể tích nước phải thêm là:
Xem thêm tại: http://loigiaihay.com/bai-4-trang-151-sgk-hoa-hoc-8-c51a10352.html#ixzz49UQu5vYO