Cho 0,53g muối cacbonat hóa trị I tác dụng vừa hết với dung dịch HCl 3,65% thấy thoát ra 1,12ml khí (đktc) và thu được dung dịch A.
a. Xác định CTHH của muối cacbonat.
b. Tính nồng độ phần trăm dung dịch A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



n Zn= 19,5/65=0,3 (mol).
PTPƯ: Zn(0.3) + HCl(0.6) ----> ZnCl2(0.3) + H2(0,3)
mHCl=0,6.36.5=21.9(g)
a) C%HCl= 21.9/300.100%=7,3%
b) VH2=0,3.22,4=6,72(lít)
c) mH2=0,3.2=0,6(g)
mZnCl2=0,3.136=40,8(g)
mddZnCl2 =(19,5+300)-0,6=318,9(g)
C%=mZnCl2/mddZnCl2.100= 40,8/318,9.100=12,793%

Gọi M là kí hiệu nguyên tử khối của kim loại hoá trị I. Công thức muối là M 2 CO 3 . Phương trình hoá học của phản ứng :
M 2 CO 3 + 2HCl → 2 MCl 2 + H 2 O + CO 2
(2M + 60)g 22400ml
1,06g 224ml
Theo phương trình hóa học trên ta có:
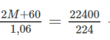
→ M = 23. Đó là muối Na 2 CO 3

gọi công thức muối là ACO3
n CO2=0,448:22,4=0,02mol
PTHH: ACO3+2HCl=>ACl2+CO2+H2O
0,02<--0,04<-0,02<-0,02->0,02
=> mHCl=0,04.36,5=1,46g
=> mddHCl=\(\frac{1,46}{10}.100=14,6g\)
ta có MACO3=2:0,02=100g/mol
=> M A=100-12-16.3=40
=> A là Ca
=> công thức muois là CACO3
ta có m CaCl2=0,02.111=2,22g
=> mddCaCl2=2+14,6-0,02.44-0,02.18=15,36g
=> C% CaCl2=2,22:15,36.100=14,45%

Đáp án D
Đặt công thức của hai muối là RCO3: x mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
x 2x x x mol
Theo định luật bảo toàn khối lượng:
mmuối cacbonat+ mHCl= m muối clorua+ mCO2+ mH2O
→ 7,0 + 2x. 36,5=9,2+ 44x+18x → x= 0,2 mol→ VCO2= 0,2.22,4= 4,48 lít

\(a,n_{CO_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ PTHH:M_2CO_3+2HCl\to 2MCl+H_2O+CO_2\uparrow\\ \Rightarrow n_{M_2CO_3}=n_{CO_2}=0,15(mol)\\ \Rightarrow M_{M_2CO_3}=\dfrac{15,9}{0,15}=106(g/mol)\\ \Rightarrow M_{M}=\dfrac{106-12-16.3}{2}=23(g/mol)\)
Vậy M là natri (Na)
\(b,n_{HCl}=2n_{CO_2}=0,3(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,3}{0,75}=0,4(l)\\ X:NaCl\\ n_{NaCl}=n_{HCl}=0,3(mol)\\ \Rightarrow C_{M_{NaCl}}=\dfrac{0,3}{0,4}=0,75M\)

gọi dd muối CO3 là ACO3
ACO3 +H2SO4 -->ASO4 +CO2+H2O
giả sử có 1 mol ACO3
=>mACO3= MA +60(g)
theo PTHH : nH2SO4=nACO3=1(mol)
=>mdd H2SO4=1.98.100/20=490(g)
nASO4=nACO3=1(mol)
=>mASO4=MA +96(g)
nCO2=nACO3=1(mol)
=>mCO2=44(g)
=>\(\dfrac{MA+96}{MA+60+490-44}\).100=24,91
giải ra ta được MA=40(g/mol0
=>ACO3:CaCO3
ta có pthh: ACO3 +H2SO4--ASO4+H2O+CO2
(A+60)g......98g.......(A+96)g..........44g
mdd H2SO4=(98.100):20=490g
mdd muối sau phản ứng=(A+60)+490-44= (A+506)g
theo đê bài ta có:C% ASO4=(A+96).100:A+506
suy ra A=40 CÓ: CTHH :CACO3

a)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2-->0,4----->0,2--->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
b) mHCl = 0,4.36,5 = 14,6 (g)
=> \(m_{dd.HCl}=\dfrac{14,6.100}{7,3}=200\left(g\right)\)
c)
mdd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
mZnCl2 = 0,2.136 = 27,2 (g)
=> \(C\%=\dfrac{27,2}{212,6}.100\%=12,8\%\)

a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, \(n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
d, \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{14,6}{7,3\%}=200\left(g\right)\)
⇒ m dd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{27,2}{212,6}.100\%\approx12,79\%\)