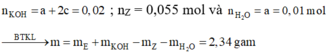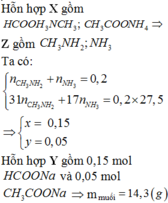Cho 23,8g hỗn hợp X gồm Cu,Fe,Al tác dụng vừa đủ với 14,56l Cl2 ở đktc thu được hỗn hợp muối Y,mặt khác cứ 0,25g mail X tác dụng với dung dịch CHo dư thu được 0,2 mail khí H2. Tính % khối lượng các kim loại trong hỗn hợp
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A.
Ta có: n Y = n H 2 = 0 , 04 m o l mol
=> E gồm các este của ancol (0,04) và các este của phenol (0,08 – 0,04 = 0,04)
mà n H 2 O = n este của phenol = 0,04 mol và n K O H = n este của ancol + 2neste của phenol = 0,12 mol
→ B T K L m E + m K O H = m muối + m ancol + m H 2 O Þ m muối = 13,7 gam

Đáp án A
Khi cho Al phản ứng với NaOH hoặc HCl thì số mol H2 thu được là như nhau:
nH2= 0,3 mol ⇒ nAl = 0,2 mol
Từ đó suy ra nH2 do Fe tạo ra = 0,4 - 0,3 = 0,1 mol
⇒nFe = 0,1 mol ⇒ nAl đã phản ứng tạo Fe là 0,1 mol vì:

⇒∑n Al trong X = 0,1 + 0,2 = 0,3mol

1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl

Chọn C.
Gọi X, Y (a mol); Z (b mol) và T (c mol).
Xét phản ứng đốt cháy: ![]()
Áp dụng độ bất bão hoà, ta có: n C O 2 - n H 2 O = a - b + 3 c = - 0 , 025 ( 2 )
Xét phản ứng với dung dịch Br2, ta có: a + 2c = 0,02 (3)
Từ (1), (2) suy ra: a = 0,01; b = 0,05 và c = 0,005.
![]() (dựa vào giá trị C trung bình)
(dựa vào giá trị C trung bình)
Xét phản ứng với KOH, ta có: