hoà tan 57,2g NaCO3 ,10H2O vào một lượng nước vừa đủ để tạo tahfnh 400 ml dd .Xác định nồng độ phần trăm và nồng độ mol của dd.Biết dung dịch này có khối lượng riêng D=1,05 g/ml
giải chi tiết giúp mik ạ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(C\%=\dfrac{30}{170}.100\%=17,647\%\)
\(V_{\text{dd}}=\left(30+170\right)1,1=220ml\)
\(n_{NaCl}=\dfrac{30}{58,5}=0,513mol\)
\(C_M=\dfrac{0,513}{0,22}=0,696M\)
\(C\%_{NaCl}=\dfrac{30}{170+30}.100\%=15\%\\ C_M=C\%.\dfrac{10D}{M}=10.\dfrac{10.1,1}{58,5}=1,88M\)

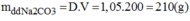
Nồng độ phần trăm của dung dịch pha chế:
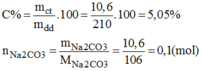
Nồng độ mol của dung dịch:
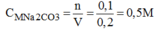

Gọi $n_{Na_2O} = 2a(mol) \Rightarrow n_{K_2O} = a(mol)$
$\Rightarrow 2a.62 + 94a = 21,8 \Rightarrow a = 0,1(mol)$
$Na_2O + H_2O \to 2NaOH$
$K_2O + H_2O \to 2KOH$
$n_{NaOH} = 2n_{Na_2O} = 0,4(mol)$
$n_{KOH} = 2n_{K_2O} = 0,2(mol)$
$C_{M_{NaOH}} = \dfrac{0,4}{0,5} = 0,8M$
$C_{M_{KOH}} = \dfrac{0,2}{0,5} = 0,4M$
$m_{dd} = D.V = 1,04.500 = 520(gam)$
$C\%_{NaOH} = \dfrac{0,4.40}{520}.100\% = 3,1\%$
$C\%_{KOH} = \dfrac{0,2.56}{520}.100\% = 2,15\%$

Ta có: \(m_{dd}=300\cdot1,05=315\left(g\right)\) \(\Rightarrow C\%_{Na_2CO_3}=\dfrac{15,9}{315}\cdot100\%\approx5,05\%\)
Mặt khác: \(n_{Na_2CO_3}=\dfrac{15,9}{106}=0,15\left(mol\right)\) \(\Rightarrow C_{M_{Na_2CO_3}}=\dfrac{0,15}{0,3}=0,5\left(M\right)\)
\(n_{Na_2CO_3}=n_{Na_2CO_3\cdot10H_2O}=\dfrac{57.2}{106+18\cdot10}=0.2\left(mol\right)\)
\(C_{M_{Na_2CO_3}}=\dfrac{0.2}{0.4}=0.5\left(M\right)\)
\(m_{Na_2CO_3}=0.2\cdot106=21.2\left(g\right)\)
\(m_{dd}=400\cdot1.05=420\left(g\right)\)
\(C\%_{Na_2CO_3}=\dfrac{21.2}{420}\cdot100\%=5.04\%\)