nung 17,8g hỗn hợp X gồm FeS và FeS2 trong bình kín chứa đầy oxi dư. Sau khi các phản ứng xảy ra hoàn toàn thu được chất rằn duy nhất là Fe2O3 và 5,6 lít SO2 (đktc)
a. tính khối lượng mỗi chất trong X
b. tính thể tích khí oxi (đktc) tối thiểu cần dùng để phản ứng hết với 17,8g hỗn hợp X


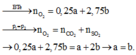
a, PT: \(4FeS+7O_2\underrightarrow{t^o}2Fe_2O_3+4SO_2\)
\(4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\)
Giả sử: \(\left\{{}\begin{matrix}n_{FeS}=x\left(mol\right)\\n_{FeS_2}=y\left(mol\right)\end{matrix}\right.\)
⇒ 88x + 120y = 17,8 (1)
Ta có: \(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PT: \(n_{SO_2}=n_{FeS}+2n_{FeS_2}=x+2y\left(mol\right)\)
⇒ x + 2y = 0,25 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,075\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{FeS}=0,1.88=8,8\left(g\right)\\m_{FeS_2}=0,075.120=9\left(g\right)\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=\dfrac{7}{4}n_{FeS}+\dfrac{11}{4}n_{O_2}=0,38125\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,38125.22,4=8,54\left(l\right)\)
Bạn tham khảo nhé!
a) Gọi nFeS = a (mol)
\(n_{FeS_2}=b\left(mol\right)\) với a; b > 0
\(n_{SO_2}=\dfrac{V}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Ta có: \(\left\{{}\begin{matrix}m_{hh}=17,8=m_{FeS}+m_{FeS_2}=88a+120b\\n_{S\left(SO_2\right)}=0,25=n_{FeS}+2n_{FeS_2}\left(bt\left[S\right]\right)=a+2b\end{matrix}\right.\)
=> a = 0,1(mol); b = 0,075(mol)
mFeS= n.M= 0,1 . 88 = 8,8(g)
=> \(m_{FeS_2}=m_{hh}-m_{FeS}=17,8-8,8=9\left(g\right)\)
b) PT:
\(4FeS+7O_2\underrightarrow{t^o}2Fe_2O_3+4SO_2\uparrow\\ 4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\uparrow\)
\(Theo2pt\Rightarrow n_{O_2}=\dfrac{7n_{FeS}+11n_{FeS_2}}{4}=0,38125\left(mol\right)\)
\(\Rightarrow V_{O_2}=n\cdot22,4=0,38125\cdot22,4=8,54\left(l\right)\)