Bài tập: Nguyên tố hoa học
2. Nguyên tử A nhẹ hơn nguyên tử B : 2 lần . Nguyên tử B nặng hơn nguyên tử X : 1, 4 lần
Nguyên tử X nặng hơn nguyên tử Oxi : 2, 5 lần
a. Hỏi A, B, X là nguyên tố gì ?
b. So sánh nặng nhẹ giữa nguyên tử A, X
c. Tính khối lượng theo g của 1 nguyên tử A
d. Tính khối lượng theo g của 6, 02. 1023 nguyên tử A,B, X và cho nhận xét
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
$2X = 5.16 \Rightarrow X = 40$
Vậy X là nguyên tố Canxi
b)
$m_{Ca} = 40.1,66.10^{-24} = 66,4.10^{-24}(gam)$
c)
$m_{5O} = 5.16.1,66.10^{-24} = 132,8.10^{-24}(gam)$
d)
$\dfrac{M_{Ca}}{M_O} = \dfrac{40}{16} = 2,5$
(nặng gấp 2,5 lần nguyên tử oxi)
$\dfrac{M_{Ca}}{M_{Cu}} = \dfrac{40}{64} = 0,625$
(nhẹ gấp 0,625 lần ngyen tử Cu)
2/
a) \(2M_X=5M_O\)
=> \(M_X=\dfrac{5.16}{2}=40\)
Vậy X là nguyên tố Canxi (Ca)
b) \(m_{Ca}=40.1,66.10^{-24}=6,64.10^{-23}\left(g\right)\)
c) \(m_O=5.16.1,66.10^{-24}=1,328.10^{-22}\left(g\right)\)
d) Nguyên tử X nặng hơn nguyên tử Oxi và nặng hơn \(\dfrac{40}{16}=2,5\left(lần\right)\)
Nguyên tử X nhẹ hơn nguyên tử Đồng và nhẹ hơn \(\dfrac{40}{64}=0,625\left(lần\right)\)

Ta có :
+) NTKO = 16 đvC
=> NTKX = 16 * 2 = 32 (đvC)
=> X là nguyên tố lưu huỳnh (S)
+) NTKMg = 24 đvC
=> NTKY = 24 * 0,5 = 12 (đvC)
=> Y là nguyên tố Cacbon (C)
+)NTKNa = 23 đvC
=> NTKZ = 23 + 17 = 40 (đvC)
=> Z là nguyên tố Canxi (Ca)
a) vì nguyên tử X nặng gấp 2 lần nguyên tử õi mà Oxi=16đvc
nên X=16*2=32(đvc)
vậy X là nguyên tố lưu huỳnh KHHH là S
b) nguyên tử Y nặng hơn nguyên tử Magie 0,5 lần mà Magie=24đvc
nên Y=24*0,5=12(đvc)
vậy Y là nguyên tố Nito KHHH là N
c) vì nguyên tử Z nặng hơn nguyên tử Natri 17đvc
mà Natri=23đvc
nên Z=23+17=40(đvc)
vậy Z là nguyên tố canxi có KHHH là Ca

Bài 2:
B = Brom : 2 = 80 : 2 = 40
=> NTK của nguyên tử B là 40 đvC
=> B là nguyên tử Canxi (Ca)
Bài 3:
X = Oxi.0,25 = 16.2,5 = 40
=> NTK của X là 40đvC
=> X là nguyên tử Canxi (Ca)
Tham Thảo :
Bài 2 Ta có: NTK B = NTK Brom / 2
=> NTK B = 80 / 2 = 40 đvC
Vậy B thuộc nguyên tố Canxi.
KHHH: Ca.

X= Oxi x2= 16x2= 32g => X là Lưu Huỳnh (S)
Y= Magie x0.5= 24x0.5= 12g => Y là Cacbon (C)
Z= Natri + 17= 23+17= 40g => Z là Canxi (Ca)

\(6NTK_A=3NTK_{Mg}\Leftrightarrow NTK_A=\dfrac{3\cdot24}{6}=12\left(đvC\right)\\ NTK_B=4+NTK_A=12+4=16\left(đvC\right)\\ NTK_C=4NTK_B=16\cdot4=64\left(đvC\right)\\ NTK_D=NTK_C-24=64-24=40\left(đvC\right)\)
Vậy A,B,C,D lần lượt là cacbon(C),Oxi(O),Đồng(Cu),Canxi(Ca)

\(a,NTK_x=2NTK_O=32\left(đvC\right)\) nên X là lưu huỳnh (S)
b, \(m_S=32\left(đvC\right)=32\cdot1,66\cdot10^{-24}=5,312\cdot10^{-23}\left(g\right)\)
c, Nguyên tử nặng hơn nguyên tử C \(\dfrac{32}{12}\approx2,7\left(lần\right)\)

a) biết nguyên tử khối của \(O=16\left(đvC\right)\)
ta có: \(X=3,5.16\)\(=56\) \(\left(đvC\right)\)
\(\Rightarrow X\) là sắt, kí hiệu là \(Fe\)
b) nguyên tử khối của \(2O\) là: \(2.16=32\left(đvC\right)\)
\(\Rightarrow X\) là lưu huỳnh, kí hiệu là \(S\)
a)Nguyên tử A là nguyên tố B(Bo) nặng 10
Nguyên tử B là nguyên tố Ne(Neon) nặng 20
Nguyên tử X là nguyên tố N(Nito)nặng 14
Cách tính ta tìm nguyên tử X trc ta lấy NTK của Oxi nhân với 2,5=14(ng tử N,lấy ng tửX nhân 1,4=20(ng tử Ne),ta lấy ng tử B tìm được chia cho 2ta đc nguyên tử Bo=10
b)So sánh nặng nhẹ :Nguyên tử B nhẹ hơn nguyên tử N =10/14=5/7 lần
Nguyên tử N nặng hơn nguyên tử B=14/10=7/5=1,4 lần
c)Khối lượng 1 g của ng tử A là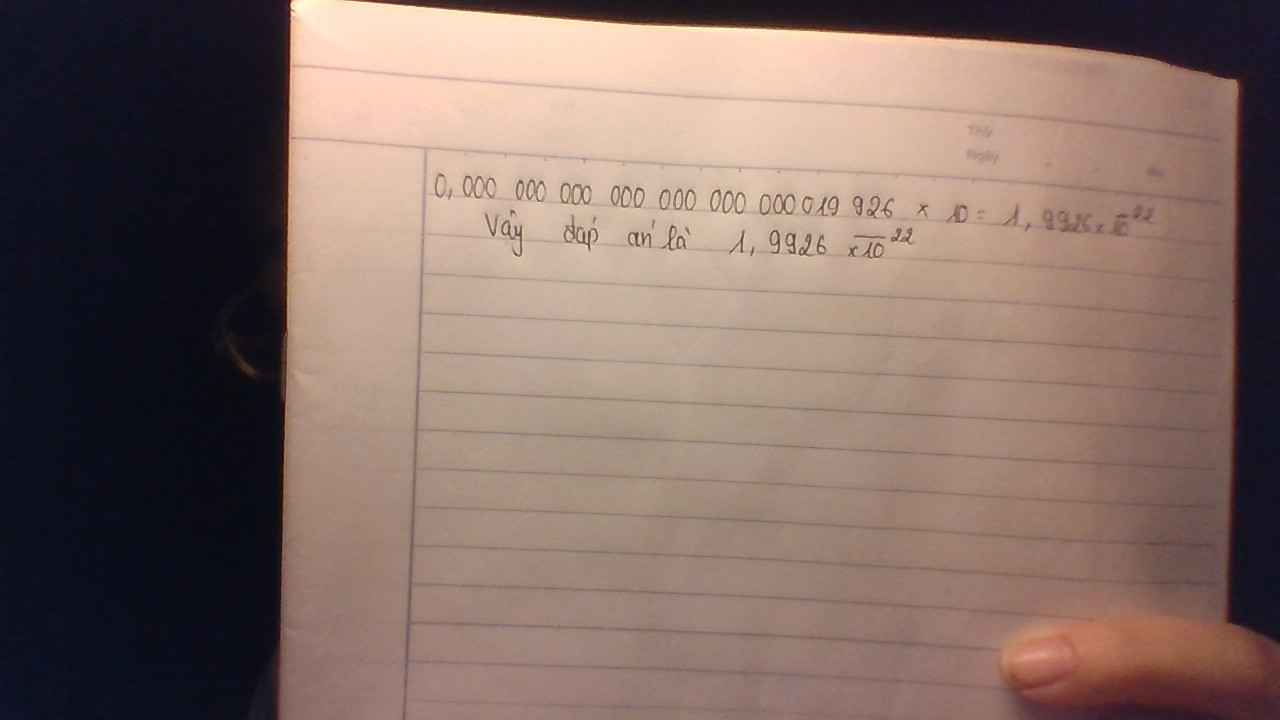
Phần cuối thì mk ko bt lm vì nó dài quá nó cg khá dễ mk chắc bn có thể lm đc